2015-05-28
CRISPR技术自2013年问世以来,近几年它不仅仅常霸屏CNS,技术发展也是日新月异。5月15日重磅新闻,被评为“Nature 2017年度十大人物”的David R. Liu教授就与“基因剪刀手”张锋教授等人宣布联合创立Beam Therapeutics公司,旨在将以一种革命性的基因编辑技术开发精准的遗传疗法,治疗一系列目前还没办法彻底治愈的遗传疾病。深扒一下,便发现这项技术是被评为“Science 2017年度十大突破”的单碱基编辑技术(base editing)。那么究竟什么是单碱基编辑技术?它与经典的CRISPR技术相比,有什么区别和优势呢,尤其是在基因治疗上?本期就一起来看看!
一、CRISPR技术与碱基编辑技术原理
l CRISPR技术
CRISPR技术是从细菌和古细菌抵抗病毒或外源核酸侵染的免疫机制改进发展起来的一门基因编辑技术,其中以二类CRISPR系统CRISPR/Cas9系统最为常用。它需要一个Cas9蛋白和一条特异靶向性的sgRNA,识别并切割基因组含PAM的靶序列,产生DNA双链断裂,进而刺激机体产生内源性DNA双链断裂修复机制,即高概率的非同源末端连接修复机制(NHEJ)和低概率的同源重组修复机制(HDR)[1],如图1所示
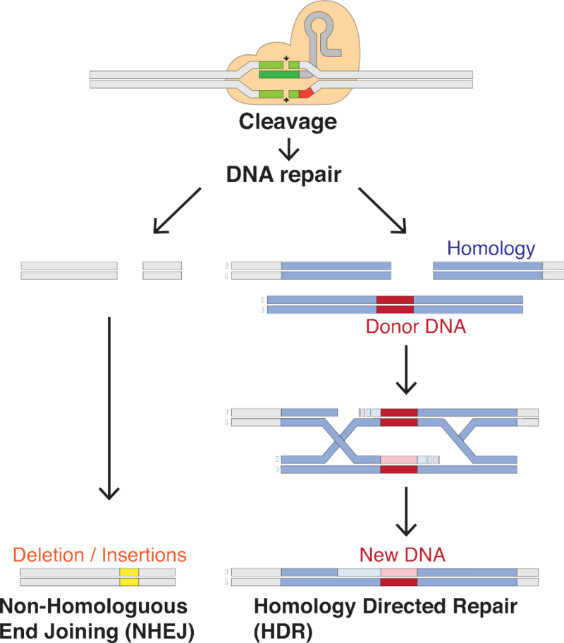
图1. CRISPR/Cas9系统的2种修复机制[1]
由于CRISPR/Cas9系统涉及到剪切 DNA 双链结构,因此可能导致不精准的基因编辑;近几年,一项建立在CRISPR/Cas9系统并可以靶向特定的单碱基的基因编辑技术相继报道,并且由于其技术的强大、高效,以及不会产生双链断裂等特点,逐渐成为人们关注的热点。
l 碱基编辑技术(base editing,BE)
定义:基于CRISPR-Cas9系统改进而来,可以针对单个DNA碱基对进行编辑;
原理:通过将失去双链切割活性的nCas9(nickase cas9,即保留单链切割活性)蛋白与脱氨基酶比如APOBEC1或者AID融合而成,既具有了dCas9结合特定DNA序列的定位能力,又具有改变碱基的能力。可在不切割双链 DNA 的情况下对靶基因位点的单个碱基进行胞嘧啶 C→胸腺嘧啶 T 或腺嘌呤A→鸟嘌呤G 的精准编辑。其中以David Liu的base editing技术应用最为广泛,如下:
2016年4月,David Liu在Nature发表第一篇单碱基编辑(CBE单碱基编辑工具)的文章:
在D10A突变的Cas9蛋白N端融合胞嘧啶脱氨酶(APOBEC),通过Cas蛋白结合靶序列后,切割与sgRNA互补的链,释放非互补链使胞嘧啶脱氨酶把编辑框内的胞嘧啶(C)突变成尿嘧啶(U),然后在DNA复制过程中被修复成胸腺嘧啶(T),这样就可以产生C-T的编辑。随后通过工具一系列的优化,最终可以实现精确的胞嘧啶(C)到胸腺嘧啶(T)的突变,即CBE单碱基编辑工具(图2a)[2]。

图2a. CBE的工作原理 [2]
2017年10月底,David Liu又发Nature发现ABE单碱基编辑工具:
他们团队通过进化筛选技术开创性地找到了一种腺嘌呤脱氨酶的突变体(TadA),同样通过融合在D10A突变的Cas9蛋白N端,把非互补链编辑框中的腺嘌呤(A)突变成次黄嘌呤(I),然后在DNA复制过程中被修复成鸟嘌呤(G),从而可以高效地把腺嘌呤(A)突变成鸟嘌呤(G),即ABE单碱基编辑工具(图2b)[3]。

图2b. ABE的工作原理[3]
二、 基因编辑技术在基因治疗中的应用
当然,技术的更新发展都是为了其应用而服务的。基因编辑技术从发现开始就被认为是未来人类疾病基因治疗的新宠,旨在为人类健康做贡献。CRISPR/Cas9基因编辑技术出现后,研究人员迅速捕捉到其对疾病基因治疗的优势,通过在疾病动物模型中的应用,CRISPR/Cas9介导的基因治疗在过去几年里已经成功在各种遗传疾病治疗中发挥作用,基因治疗也从“缺啥补啥”的过表达方式转变到“哪里错误修正哪里”的精准治疗方式。接下来,将详细介绍一下CRISPR/Cas9基因编辑技术和单碱基编辑技术在基因治疗中的应用。
l CRISPR/Cas9基因编辑技术介导的基因治疗
原理:CRISPR/Cas9主要是通过两种策略应用于疾病治疗的:一是,通过NHEJ的方式来破坏突变的致病基因或删除突变蛋白中的突变结构域 (图3);二是,通过HDR的方式人为提供正确的修复模板来精确的修复致病基因的突变位点(图4)。
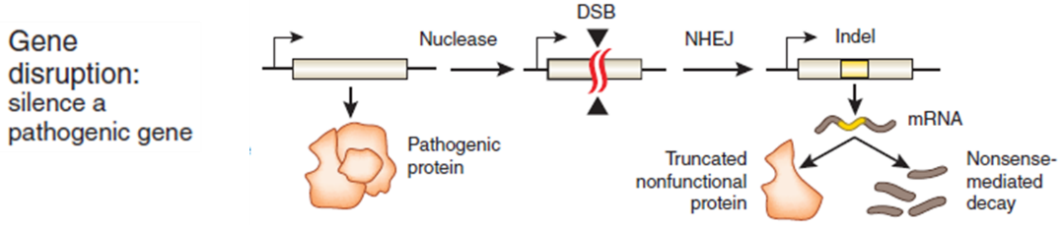
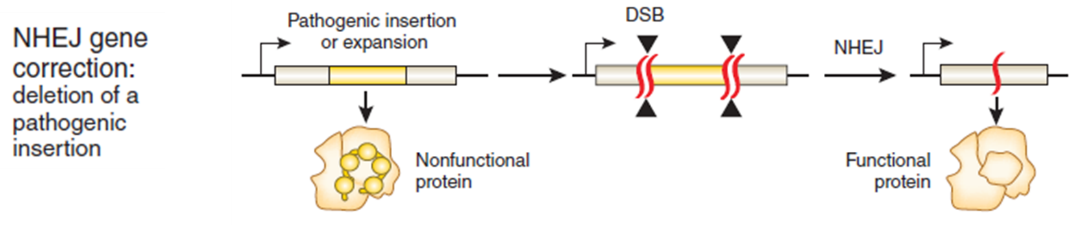
图3. 基因治疗策略:NHEJ方式介导的基因治疗(来源张锋)
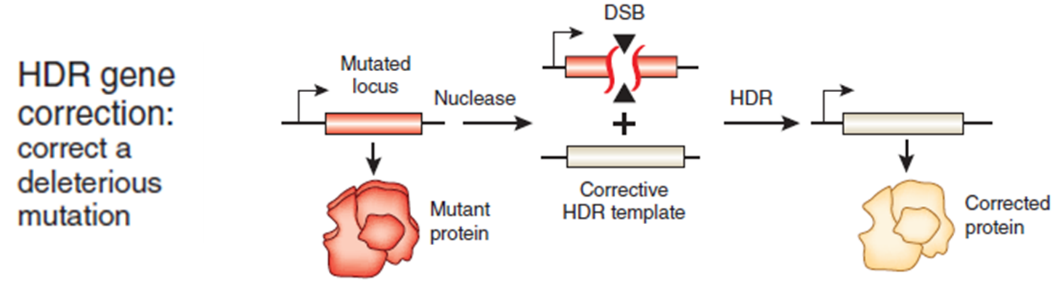
图4. 基因治疗策略:HDR方式介导的基因治疗(来源张锋)
最新研究进展:
一)NHEJ的方式来破坏突变的致病基因或删除突变蛋白中的突变结构域:
1. 2016年年初,三篇Science同时报道通过CRISPR/Cas9技术删除患有杜式肌肉营养不良的疾病小鼠(DMD)基因突变的外显子,产生缩短但仍能发挥作用的新版本抗肌萎缩蛋白,成功治愈了小鼠的杜式肌肉营养不良疾病[4-6];
2. 2017年5月,JCI报道通过AAV递送CRISPR/Cas9系统,成功删除亨廷顿舞蹈症致病基因的CAG重复序列[7];
3. 2017年11月,Nature报道通过脂质体递送CRISPR/Cas9系统到耳朵中,敲除疾病小鼠耳细胞中显性突变基因Tmc1,成功治愈常染色体显性遗传的听力丧失遗传病[8];
……
毕竟对于以上这类可以通过直接删除致病基因的方式治疗的疾病还是占少数的,而对于大多数遗传疾病,尤其是代谢酶突变导致的疾病,基本上是不能通过直接删除致病基因的方式去治疗疾病的,它需要精确的修复致病突变才能恢复疾病表型,达到治疗效果。因此,这就需要HDR介导的基因治疗方式来精确的修复致病基因的突变位点。
二)HDR的方式精确的修复致病基因的突变位点:
1. 2016年2月,NBT报道通过两个AAV分别递送CRISPR/Cas9系统和修复模板,在疾病小鼠模型上,成功治愈了由鸟氨酸转氨甲酰酶(OTC)突变导致的高血氨症,研究表明,通过这样的策略可以在幼鼠中修复效率达到10%左右[9];
2. 同期,NBT也报道了通过AAV递送修复模板,纳米材料递送CRISPR/Cas9系统的策略,同样在疾病小鼠模型上,成功地治愈了Fah突变导致的一型络氨酸血症,并且通过纳米材料的递送方式可以降低脱靶(off-target)效率[10]。
……
虽然CRISPR/Cas9系统介导的疾病基因治疗在动物模型上的研究令人兴奋,但还是具有其目前无法解决的弊端,尤其是CRISPR/Cas9系统介导HDR的方式来精确的修复致病基因的突变位点的基因治疗策略。首先,对于大多数疾病来说,它需要非常高HDR效率才可能缓解疾病表型,而目前体内HDR的效率的确非常之低;其次,CRISPR/Cas9系统引起DNA双链断裂后,机体更倾向于NHEJ的修复方式,这就会使基因组在on target的位置附近产生更多的原来没有的插入和缺失(indel);最后,也是研究人员最为关注的CRISPR/Cas9系统的脱靶问题。
l 单碱基编辑技术介导的基因治疗前景可观!
研究统计结果表明,在已知的与疾病相关的50000种人类基因变异中,有超过30000种基因突变都是由于单碱基的改变而导致疾病的(图5)。因此,利用高编辑效率、不产生DNA双链断裂的单碱基编辑工具来进行遗传疾病的基因治疗是非常具有应用价值的。

图5. 人类遗传病中单碱基突变类型(来源David Liu)
2018年4月27日,NBT报道了利用单碱基编辑系统ABE成功治愈了杜式肌肉营养不良疾病小鼠,通过AAV递送ABE系统到肌肉组织,将其一个致病的终止密码子给突变成正常氨基酸谷氨酰胺(Gln),抗肌萎缩蛋白(dystrophin)的表达提高了17%左右,并且没有检测到任何off target发生(图6)[11]。

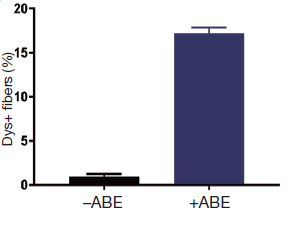
图6. ABE系统介导的杜式肌肉营养不良疾病的基因治疗 [11]
由于单碱基编辑技术近2年才开始浮出水面,因此相关的进展还比较少,但是我们相信,单碱基编辑技术作为近年来具有突破性进展的颠覆性技术,相信经过科学家们的不断努力,在未来终将为人类疾病的治疗做出贡献。
邦耀生物作为一家高新技术企业,有幸参与其中,也致力于利用基因治疗(包括单碱基编辑技术)攻克各种遗传疾病(如地中海贫血症、B型血友病等),并且已在该领域成功申请多项专利。目前不仅具有成熟构建疾病动物模型的经验(尤其是点突变的疾病模型);并且邦耀已经在多种遗传疾病如B型血友病和Ⅰ型酪氨酸血症等动物疾病模型上初步实现了体内基因治疗,有效控制了疾病进展[12-13];相关技术也申请了多项专利。同时邦耀结合自身在基因编辑、免疫学领域的强大技术实力和科研团队,已成功构建通用性CAR-T的研发转化平台,目前正在开展通用性CAR-T的系列转化研究。
邦耀生物作为一家高新技术企业,有幸参与其中,也致力于利用基因治疗(包括单碱基编辑技术)攻克各种遗传疾病(如地中海贫血症、B型血友病等)。目前不仅具有成熟构建疾病动物模型的经验(尤其是点突变的疾病模型);并且我们已经在多种遗传疾病如B型血友病和Ⅰ型酪氨酸血症等动物疾病模型上初步实现了体内基因治疗,有效控制了疾病进展[12-13];同时我们结合自身在基因编辑、免疫学领域的强大技术实力和科研团队,已成功构建通用型CAR-T的研发与转化平台,并在全球率先启动开展通用型人源化CD19-CART免疫细胞治疗(Universal CAR-T)的系列临床试验。最后,希望可以和各位科学界同仁一起,不断去突破并优化技术,治愈更多遗传疾病患者。
已按照GMP生产标准搭建了成熟的通用型CAR-T研发与转化平台,利用最先进的基因编辑技术构建了靶向多种肿瘤的安全性更高、治疗效果更好的通用型CART细胞产品,并在国内率先开展了一系列以人源化CD19-CART为代表的通用型免疫细胞治疗(Universal CAR-T)的临床试验。
参考文献:
【1】 Patrick D. Hsu,Eric S. Lander,and Feng Zhang. Development and Applications of CRISPR-Cas9 for Genome Engineering. Cell,2014, 157(6):1262-78.
【2】 Alexis C. Komor1, Yongjoo B. Kim, Michael S. Packer,et al. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage.nature,2016, 533(7603):420-4.
【3】 Nicole M. Gaudelli, Alexis C. Komor, Holly A. Rees,et al. Programmable base editing of A•T to G•C in genomic DNA without DNA cleavage.nature,2017, 551(7681):464-471.
【4】 Mohammadsharif Tabebordbar, Kexian Zhu, Jason K. W. Cheng,et al. In vivo gene editing in dystrophic mouse muscle and muscle stem cells.science,2016, 351(6271):407-411.
【5】 Christopher E. Nelson, Chady H. Hakim, David G. Ousterout,et al. In vivo genome editing improves muscle function in a mouse model of Duchenne muscular dystrophy.science,2016, 351(6271):403-7.
【6】 Chengzu Long, Leonela Amoasii, Alex A. Mireault,et al. Postnatal genome editing partially restores dystrophin expression in a mouse model of muscular dystrophy.science,2016, 351(6271):400-3.
【7】 Su Yang, Renbao Chang, Huiming Yang,et al. CRISPR/Cas9-mediated gene editing ameliorates neurotoxicity in mouse model of Huntington’s disease.jci,2017, 127(7):2719-2724.
【8】 Xue Gao, Yong Tao, Veronica Lamas, et al. Treatment of autosomal dominant hearing loss by in vivo delivery of genome editing agents.nature,2017, 553(7687):217-221.
【9】 Yang Yang, Lili Wang, Peter Bell,et al. A dual AAV system enables the Cas9-mediated correction of a metabolic liver disease in newborn mice.nbt,2016, 34(3):334-8.
【10】 Hao Yin, Chun-Qing Song, Joseph R Dorkin, et al. T herapeutic genome editing by combined viral and non-viral delivery of CRISPR system components in vivo.nbt,2016, 34(3):328-33.
【11】 Seuk-Min Ryu, Taeyoung Koo, Kyoungmi Kim,et al. Adenine base editing in mouse embryos and an adult mouse model of Duchenne muscular dystrophy.nbt,2018.
【12】 Yuting Guan, Yanlin Ma, Qi Li2, et al. CRISPR/Cas9-mediated somatic correction of a novel coagulator factor IX gene mutation ameliorates hemophilia in mouse. EMBO Molecular Medicine,2016, 8(5):477-88.
【13】 Shao Y, Wang L, Guo N, at al. Cas9-nickase-mediated genome editing corrects hereditary tyrosinemia in rats. J Biol Chem,2018, 293(18):6883-6892.