2020-05-11
2020年5月11日,上海邦耀生物科技有限公司(下称邦耀生物)与华东师范大学密切合作,为打破现有碱基编辑技术效率瓶颈,通过融合单链DNA结合蛋白的功能域开发了一系列超高活性的新型胞嘧啶碱基编辑器(命名为:hyCBE)。相对于已报道的CBE,在人类细胞系及小鼠胚胎中其活性均显著提高并可以编辑到靠近PAM区的碱基。更令人振奋的是,活性的提高并没有增加DNA及RNA脱靶风险,并且在基因治疗等表现出非常广阔的应用前景。相关成果于2020年5月11日在线发表于国际著名学术期刊Nature Cell Biology。这也是邦耀生物继发表在 Cell Research、Nature Medicine 等期刊的基因治疗重磅成果后,在基因编辑领域开发核心碱基编辑工具的开篇之作。

据ClinVar数据显示,人类的遗传病中58%是由于单个碱基突变引起的。虽然Cas9激活的同源重组可以实现对突变位点的精确修正,但效率非常低(0.1%~5%),严重阻碍了其应用。而通过将胞嘧啶脱氨酶与nickase Cas9(D10A)融合而成的胞嘧啶碱基编辑器BE3(Cytosine base editor, CBE),在不引入DNA双链断裂同时也不需要重组修复模板的情况下对编辑窗口(距离PAM远端起的第4-7位)内的胞嘧啶脱氨,实现C>T的碱基转换,具有更加安全、高效、精准的特点。在基因治疗,农作物遗传育种,药物筛选等领域展示了广泛的应用前景。
自CBE被报道以来,已有多种策略对其进行了优化改进。例如在提高活性方面,主要是通过密码子优化及增加更强的核定位信号、用高活性的胞嘧啶脱氨酶APOBEC3A或Anc689替换APOBEC1、融合额外的UGI增加编辑效率和产物纯度。而通过对脱氨酶的分子进化获得的evoAPOBEC1-BE4max大幅提高针对GC motif中胞嘧啶的编辑效率。虽然这些方法一定程度上提高了CBE的活性,但是对于编辑窗口的影响不大,特别是更靠近PAM序列的碱基仍然很难被编辑到。因此,是否有新的策略可以提高编辑活性而又能扩增靶向碱基的范围,一直是碱基编辑器优化的难点。
由于CBE主要是以单链DNA(ssDNA)为底物,因此研究团队猜测如果增强脱氨酶与ssDNA的结合能力,是否能增加脱氨酶作用时间而增强活性呢?于是,通过对10个非序列特异性的ssDNA结合结构域(ssDBD)与CBE进行融合,通过筛选,发现将Rad51蛋白的ssDBD融合到APOBEC1与Cas9n之间能显著提高碱基编辑活性,同时编辑窗口也大幅增加(图1)。通过10个靶点的分析,在编辑窗口C4-C8中,hyBE4max比BE4max活性提高了1.5-2倍,而在C9-C15这些更靠近PAM的碱基中,活性最多提高了18倍。
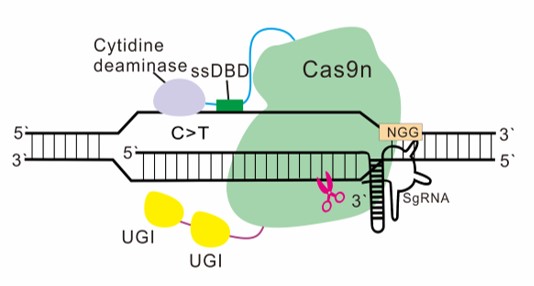
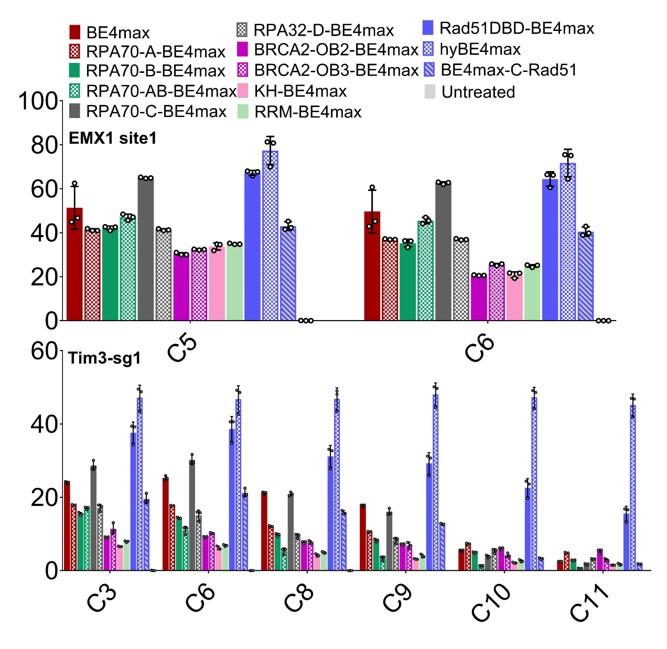
图1. hyCBE模式图及对不同ssDBD的筛选结果
为了验证融合ssDBD的策略是否具有通用性,用类似的方法改造A3A-BE4max和特异性识别TC motif中C碱基的eA3A-BE4max,获得了hyA3A-BE4max和hyeA3A-BE4max。通过大量的实验证明,相比A3A-BE4max,hyA3A-BE4max活性在C3-C11位点提高了1.2-2倍,C12-C17位点活性提高3-4倍,通过小鼠胚胎显微注射也进一步证明其在编辑更靠近PAM序列的碱基的独特优势。与eA3A-BE4max相比,hyeA3A-BE4max仍然能非常特异性地靶向TC motif中的C,编辑窗口由C4-C9拓展为C4-C15,活性最高提高了257倍;而在小鼠胚胎中靶向Dmd基因时,C13位点编辑效率也大大提高,F0小鼠平均编辑活性提高了近60倍,F0代小鼠获得Dmd纯合点突变的效率达到40%。
论文进一步验证hyCBEs特别是hyeA3A没有检测到DNA或者RNA层面的脱靶,具有非常高的精准性。最后,通过比较多种CBE在编辑胎儿血红蛋白(HBG1/2)启动子-117位点的能力发现,hyeA3A能在红细胞前体细胞系中精确催化-117G>A的转换,而与周围同时发生碱基突变(bystander mutation)的细胞相比,具有更高的HBG表达水平,展示了hyeA3A-BE4max对于精准治疗β-血红蛋白病的巨大潜力。该工作开发了能提高编辑活性及拓宽靶点范围的一系列新的CBE,为基础研究与基因治疗提供了新的优化工具。
据了解,今年1月份,刘明耀教授和李大力教授团队已经率先证明单碱基编辑器编辑技术靶向HBG启动子激活胎儿期血红蛋白的表达,对于治疗β地中海贫血的可行性与有效性,相关研究发表在国际著名学术期刊Cell Research;同年3月份国际著名学术期刊Nature Medicine又在线发表了邦耀生物科学家吴宇轩博士证明单碱基编辑技术可以靶向BCL11A的红系增强子原件激活胎儿期血红蛋白,或者编辑β血红蛋白基因的特定突变,有望通过编辑自体造血干细胞治疗包括β地贫在内的β血红蛋白病。而最新自主研发的hyCBEs系列工具拥有更高的编辑活性和更宽的编辑窗口,对于β血红蛋白病的治疗具有更大的优势。邦耀生物正着力围绕这几项自主技术开展临床转化。
据统计,在我国β-地中海贫血的患病率是2.21%,其类型达48种。基因编辑技术介导的基因治疗是精准医学领域的一大突破,利用单碱基编辑技术重新激活胎儿血红蛋白的表达,也为β-地中海贫血的个性化治疗提供了可能性。
邦耀生物联合创始人、总裁席在喜先生透露:邦耀生物已搭建了创新、高效的基因编辑平台,今天开发的超高活性的单碱基编辑器将会为基因治疗再添利器,邦耀生物着眼于基因药物和细胞药物的开发,目前已与国内多家医疗单位合作,在遗传疾病及恶性肿瘤的研究中取得了阶段性突破。除坚实的基础研发实力外,邦耀生物还拥有经验丰富的工艺研发与生产团队及6000平米GMP级别中试基地,能够将创新成果及时迅速进行转化并推向临床!邦耀生物布局于划时代的基因与细胞药物领域,并致力于改写和引领中国新一代药企在全球生命科技领域格局!